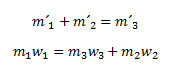Roztoky
Roztoky sú homogénne zmesi dvoch alebo viacerých látok. Majú premenlivé zloženie v závislosti od vzájomnej rozpustnosti zložiek sústavy. Každý roztok obsahuje rozpúšťadlo a v ňom rozpustenú látku. Zvyčajne platí, že so zvyšujúcou sa teplotou stúpa množstvo látky, ktoré je možné v rozpúšťadle rozpustiť (so zvyšujúcou sa teplotou stúpa rozpustnosť látky).
Zloženie roztokov môžeme vyjadriť nasledovnými spôsobmi:
Hmotnostný zlomok wB udáva aká hmotnosť zložky B pripadá na jednotkovú hmotnosť roztoku:
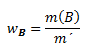
kde m(B) je hmotnosť zložky B, m´ je hmotnosť roztoku.
Hmotnostné percento vyjadruje, aká hmotnosť zložky B sa nachádza v 100 g (kg) roztoku. Je určené podielom hmotnosti zložky B a roztoku vynásobeným stomi:
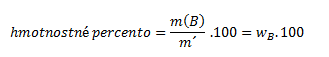
Objemový zlomok φB udáva objem látky B pripadajúci na jednotkový objem roztoku: udáva objem látky B pripadajúci na jednotkový objem roztoku:
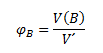
Objemové percento vyjadruje aký objem zložky B sa nachádza v 100 ml (l) roztoku: vyjadruje aký objem zložky B sa nachádza v 100 ml (l) roztoku:
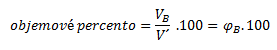
Molový zlomok xB vyjadruje aké látkové množstvo zložky B pripadá na jednotkové látkové množstvo všetkých zložiek roztoku:
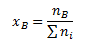
Koncentrácia látky (koncentrácia látkového množstva, molarita) cB, ktorá sa zjednodušene označuje M., ktorá sa zjednodušene označuje M.
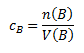
Molita látky mB vyjadruje látkové množstvo látky B rozpustené v 1 kg rozpúšťadla: vyjadruje látkové množstvo látky B rozpustené v 1 kg rozpúšťadla:
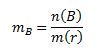
kde m(r) je hmotnosť rozpúšťadla vyjadrená v kg; jednotkou molality je mol.kg-1
Pri zvažovaní hmotnostných bilancií v roztokoch berieme do úvahy nasledujúce situácie:
- a.) Riedenie roztoku pridaním čistého rozpúšťadla: Zvyšujeme tým hmotnosť roztoku, no celková hmotnosť rozpustenej látky ostáva konštantná. Pri výpočte zloženia výsledného roztoku, prípadne potrebného množstva východiskového roztoku používame postup tzv. bilancovania hmotnosti rozpustenej látky. Načrtneme si schému prípravy výsledného roztoku, do systému pridávame vodu s nulovou koncentráciou rozpustenej látky a roztok s konkrétnou koncentráciou rozpustenej látky:
Bilančná schéma:
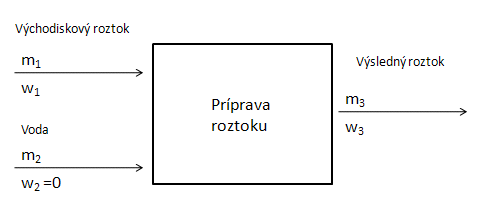
Využívame nasledujúcu rovnicu:

- b.) Príprava roztoku zmiešaním dvoch rôzne koncentrovaných roztokov: Výsledná hmotnosť roztoku m´3 je daná súčtom hmotností zmiešavaných roztokov. Množstvo rozpustenej látky je taktiež dané súčtom hmotností látok vo východiskových roztokoch:
Bilančná schéma:
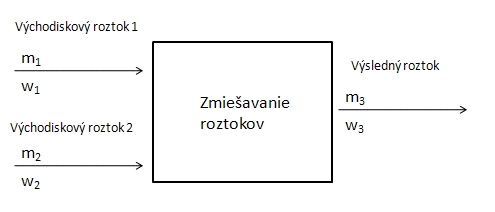
Využívame nasledujúcu rovnicu:
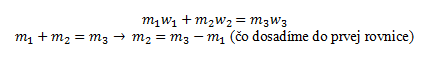
- c.) Príprava roztoku odparením rozpúšťadla: Znižujeme celkovú hmotnosť roztoku, ale množstvo rozpustenej látky ostáva rovnaké:
Bilančná schéma:

Využívame nasledujúcu rovnice:
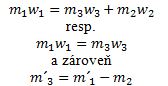
- d.) Príprava roztoku kryštalizáciou: Ochladením roztoku sa zníži rozpustnosť, prebytočná látka sa z roztoku vylúči vo forme kryštálov:
Bilančná schéma:

Využívame nasledujúcu rovnice: