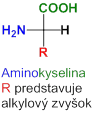
Aminokyseliny
Ako vidíme vo všeobecnom vzorci aminokyselín, ich α-uhlík je chirálne centrum molekuly, pretože má všetky 4 substituenty rôzne a tie sa môžu rôzne usporiadať v priestore, aj keď sumárny vzorec aminokyseliny ostane totožný. Samozrejme okrem glycínu, ten má na tomto uhlíku dva rovnaké substituenty, vodíky.
Aminokyseliny v bielkovinách majú L-konfiguráciu, to znamená, že aminokyselina sa v tomto špeciálnom zápise nacháza vľavo:
D-aminokyseliny sa považujú za „neprirodzené“ a boli nájdené iba v niektorých peptidových antibiotikách a bunkovej stene niektorých baktérií.
Aby sa v aminokyselinách vedci lepšie vyznali, priradili každej proteinogénnej aminokyseline troj- a jednopísmenový kód.
| AMK | 3 písmenový kód | 1 písmenový kód |
| Nepolárne hydrofóbne | ||
| glycín | Gly | G |
| alanín | Ala | A |
| valín | Val | V |
| leucín | Leu | L |
| izoleucín | Ile | I |
| metionín | Met | M |
| fenylalanín | Phe | F |
| tryptofán | Trp | W |
| prolín | Pro | P |
| AMK | 3 písmenový kód | 1 písmenový kód | |
| polárne záporne nabité | |||
| lyzín | Lys | K | |
| arginín | Arg | R | |
| histidín | His | H | |
| polárne kladne nabité | |||
| kyselina asparágová | Asp | D | |
| kyselina glutámová | Glu | E | |
| | | | |
| AMK | 3 písmenový kód | 1 písmenový kód |
| polárne hydrofilné | ||
| serín | Ser | S |
| treonín | Thr | T |
| cysteín | Cys | C |
| tyrozín | Tyr | Y |
| asparagín | Asn | N |
| glutamín | Gln | Q |
V roztoku je aminoskupina intramolekulovo (teda v rámci jednej a tej istej molekuly) neutralizovaná protónom karboxylovej skupiny. Vzniká teda tzv. zwitterión (ión majúci kladný aj záporný náboj súčasne, tiež amfión). Ak sa aminokyselina nachádza v kyslom roztoku bohatom na H+ ióny (nízke pH), dochádza k ďalšej protonizácii karboxylovej skupiny. Aminokyselina sa tým dostane do protonizovaného stavu, v ktorom má kladný celkový náboj. Ak sa naopak zwitteión dostane do roztoku s vysokým pH, teda do zásaditého roztoku, dochádza k deprotonizácii NH3+ skupiny (teda k strate H+) a aminokyselina sa dostane do deprotonizovaného stavu, v ktorom je záporne nabitá.
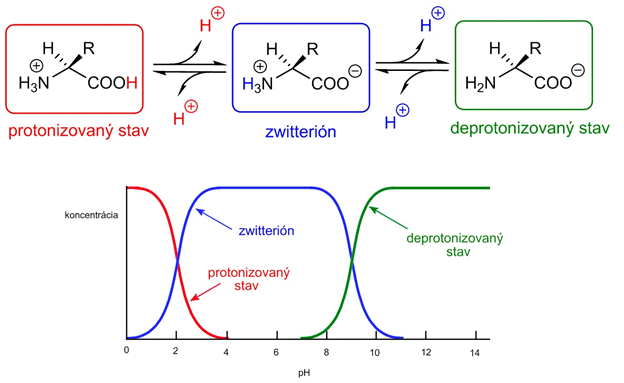
Obrázok- koncentrácia ionizačných stavov aminokyseliny ako závislosť od pH roztoku.
V zásaditom roztoku s vysokým pH sa aminokyseliny nachádzajú a správajú ako anióny. V kyslom roztoku s nízkym pH ako katióny. Hodnota pH, pri ktorej je molekula aminokyseliny (ale aj peptidu alebo bielkoviny) neutrálna a vyskytuje sa vo forme zwitteriónu, sa nazýna izoelektrický bod a je rôzna pre každú aminokyselinu (peptid/ bielkovinu).
Zaujímavosť:
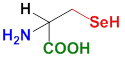
Existuje ešte jedna proteinogénna aminokyselina, selenocysteín, ktorá ma miesto síry v –SH skupine atóm selénu. Na rozdiel od cysteínu má nižšiu hodnotu pK a vyšší redukčný potenciál, preto je súšasťou antioxidačných selenoproteínov ako napr. Glutationperoxidáza, tioredoxínreduktáza, formátdehydrogenáza, glycínreduktáza, niektorých hydrogenáz. Na to, aby sa zaradil do peptidového reťazca týchto enzýmov musí byť špeciálne kódovaný v DNA, musí mu predchádzať asi 60 nukleotidov dlhá sekvencia nazývaná SECIS element (z angl. SelenoCysteine Insertion Sequence element).
1. K aminokyseline priradťe správny typ alkylového reťazca:
a) lyzín 1) zásaditý
b) serín 2) kyslý
c) cysteín 3) obsahuje kyslík
d) leucín 4) nepolárny alifatický
e) kyselina asparágová 5) obsahuje síru
Riešenie:
- a-1
- b-2
- c-5
- d-4
- e-2
2.Pri akom pH sa nachádzajú tieto aminokyseliny?
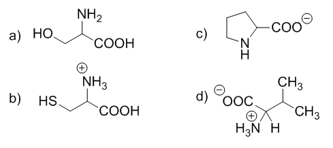
Riešenie:
a) molekula je ako celok neutrálna, žiadna skupina nie je protonizovaná ani deprotonizovaná. Nachádza sa v neutrálnom pH.
b) Molekula obsahuje nedisociovanú karboxylovú skupinu a protonizovanú aminoskupinu. Nachádza sa preto v prostredí bohatom na H+ ióny, teda v kyslom prostredí s nízkym pH.
c) aminokyselina má deprotonizovanú karboxylovú skupinu, nachídza sa teda v zásaditom prostredí s vysokým pH.
d) Molekula sa nachádza v roztoku ako zwitterión, nachádza sa preto vo svojom izoelektrickom bode, ktorý je pre uvedený valín pH 6,02.
3. Charakterizujte uvedenú aminokyselinu:
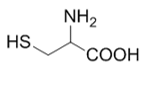
Aminokyselina obsahuje jednu aminoskupinu a jednu karboxylovú skupinu, obe v neutrálnej forme. Tioskupina v postrannom reťazci nevplýva na kyslé ani zásadité vlastnosti molekuly.
4. Ktorá z uvedených aminokyselín nie je opticky aktívna?
- a) treonín
- b) valín
- c) serín
- d) glutamín
- e) glycín
- f) lyzín
5.Koľko aminokyselín sa bežne vyskytujú v bielkovinách?
- a) 300
- b) 20
- c) 40
- d) 5
6. Všetky uvedené aminokyseliny sú alifatické okrem:
- a) glycín
- b) histidín
- c) lyzín
- d) alanín
- e) kyselina asparágová
- f) prolín
7.Ktoré tvrdenie o izoelektrickom bode je správne:
- a) hodnota pH, pri ktorej sa aminokyselina v elektrickom poli nepohybuje
- b) hodnota pH, pri ktorej sa aminokyselina pohybuje ku katóde
- c) hodnota pH, pri ktorej sa aminokyselina pohybuje k anode
- d) hodnota pH, pri ktorej sa aminokyselina vyskytuje v podobe amfiónu
8.Ktoré tvrdenie o izoelektrickom bode je správne:
- a) izoelektrický bod vyjadruje určitú špecifickú hodnotu pH
- b) izoelektrický bod závisí od funkčných skupín molekuly
- c) izoelektrický bod závisí od molekulovej hmotnosti aminokyseliny
- d) izoelektrický bod majú iba aminokyseliny
- e) izoelektrický bod je rovnaký pre všetky bielkoviny
- f) izoelektrický bod je charakteristický znak každej aminokyseliny
9. Kyselina asparágová je:
- a) monoamino dikarboxylová kyselina
- b) diamino monokarboxylová kyselina
- c) aromatická aminokyselina
- d) iminokyselina
10. Vymenujte a nakreslite aminokyseliny obsahujúce síru.
Pro zobrazení řešení se přihlaste.