Rovnice beze změny oxidačního čísla
Neredoxné rovnice sú rovnice chemických reakcií, pri ktorých nedochádza k zmene oxidačného čísla žiadneho atómu. Na zisťovanie stechiometrických koeficientov v rovniciach neredoxných reakcií sa nedá použiť žiadny jednoduchý a zároveň univerzálny algoritmus. Chemici pristupujú k riešeniu neredoxných rovníc zo začiatku väčšinou metódou pokus-omyl, neskôr vylepšenou empíriou, teda na základe skúseností. Riešenie však vždy musí vyhovovať všeobecným pravidlám na výpočet stechiometrických koeficientov. 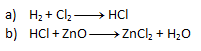
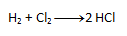
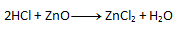
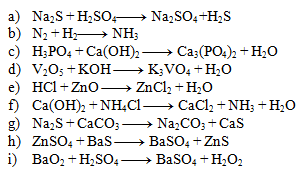
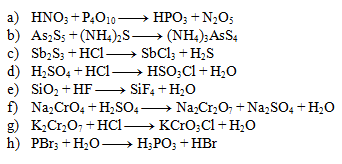
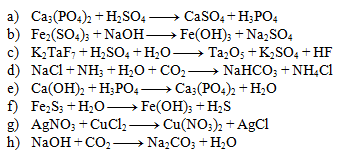
Pro zobrazení řešení se přihlaste.
Pro zobrazení řešení se přihlaste.
Pro zobrazení řešení se přihlaste.
Pro zobrazení řešení se přihlaste.
Pro zobrazení řešení se přihlaste.
Pro zobrazení řešení se přihlaste.
- Na začiatku nájdeme v chemickej rovnici látku (reaktant alebo produkt), ktorej vzorec má najväčšie stechiometrické indexy (resp. obsahuje najväčší počet atómov). Stechiometrický koeficient tejto látky budeme považovať za jednotkový.
- Potom pridáme koeficienty pred látky, ktoré obsahujú rovnaké atómy ako látka s prideleným jednotkovým koeficientom (podľa pravidla bilancie počtu atómov, prípadne podľa pravidla bilancie nábojových čísiel).
- Postupne pridávame koeficienty pred látky, ktoré ešte nemajú priradené koeficienty na základe počtu atómov v látkach, ktoré už koeficienty majú (opäť podľa pravidla bilancie počtu atómov, prípadne podľa pravidla bilancie nábojových čísiel).
- Ako predposledné zisťujeme počty atómov vodíka a podľa potreby doplníme stechiometrické koeficienty.
- Ako posledné zistíme počty atómov kyslíka na oboch stranách rovnice. Táto operácia nám obvykle slúži na kontrolu už získaných koeficientov.
1. Vyčíslite nasledujúce chemické rovnice:
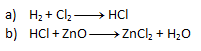
Riešenie:
- a) Na ľavej strane sa chlór aj vodík nachádzajú po dvakrát. Podľa zákona zachovania počtu atómov sa musí rovnaký počet nachádzať aj na pravej strane, preto napíšeme pred HCl číslo 2. Výsledná rovnica teda vyzerá takto:
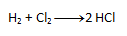
- b) Na pravej strane sa chlór nachádza dvakrát, no na ľavej strane len raz. Preto napíšeme pred HCl číslo 2. Počet ostatných prvkov potom „sedí“ na oboch stranách.
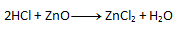
2. Vyčíslite nasledujúce chemické rovnice:
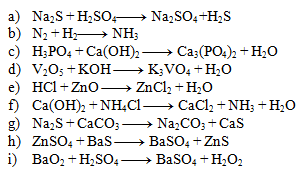
Riešenie:
- a) 1,1,1,1
- b) 1,3,2
- c) 2,3,1,6
- d) 1,6,2,3
- e) 2,1,1,1
- f) 1,2,1,2,2
- g) 1,1,1,1
- h) 1,1,1,1
- i) 1,1,1,1
3.Doplňte stechiometrické koeficienty pri nasledujúcich rovniciach:
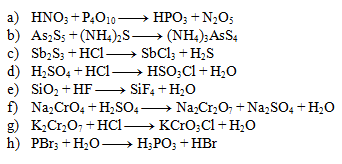
Riešenie:
- a) 4,1,4,2
- b) 1,3,2
- c) 1,6,2,3
- d) 1,1,1,1
- e) 1,4,1,2
- f) 2,1,1,1,1
- g) 1,2,2,1
- h) 1,3,1,3
4. Doplňte stechiometrické koeficienty do rovníc:
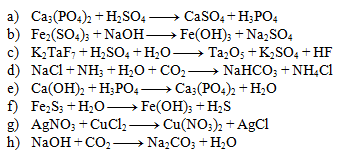
5. Zistite stechiometrické koeficienty v rovnici:
H3PO4 + CaCO3 → Ca3(PO4)2 + CO2 + H2O
6. Zistite stechiometrické koeficienty v tejto rovnici:
V2O5 + HF + KOH + H2O2 + → K3[V2O2(O2)3F3]•HF•2H2O + H2O
7. Zistite stechiometrické koeficienty v tejto rovnici:
K2SO4 + Cr2O3 + H2SO4 + H2O → KCr(SO4)2•12H2O
8. Zistite stechiometrické koeficienty v nasledujúcej chemickej rovnici:
P4O10 + H2O → H3PO4
9. Zistite stechiometrické koeficienty v nasledujúcej chemickej rovnici:
HCOOH + MgO → (HCOO)2Mg + H2O