Isoprozesse
1. Was sind Isoprozesse?
Lösung:
Isoprozesse sind Vorgänge in einem idealen Gas mit konstanter Masse, bei denen eine der Zustandsgrößen konstant bleibt.
A) Isothermer Prozess (T = konstant)
Boyle-Mariotte-Gesetz
Die bei einem isothermen Prozess von einem idealen Gas aufgenommene Wärme wird zur Verrichtung von Arbeit verwendet.
B) Isochorer Prozess (V = konstant)
Gesetz von Charles
Die bei einem isochoren Prozess von einem idealen Gas aufgenommene Wärme wird zur Erhöhung seiner inneren Energie genutzt.
C) Isobarer Prozess (p = konstant)
Gay-Lussac-Gesetz
Die bei einem isobaren Prozess von einem idealen Gas aufgenommene Wärme wird sowohl zur Änderung der inneren Energie als auch zur Verrichtung von Arbeit verwendet.
D) Adiabatischer Prozess (Q = 0) – es findet kein Wärmeaustausch zwischen dem Gas und der Umgebung statt. p,V,T können sich ändern.
Poisson-Gesetz
2.Welches Volumen werden 30 Liter Luft haben, wenn wir bei gleicher Temperatur den Druck von 72 kPa auf 75 kPa erhöhen?
Lösung:
Analyse:
V1 = 30 l = 30·10-3 m3, p1 = 72·103 Pa, p2 = 75·103 Pa, V2 = ?
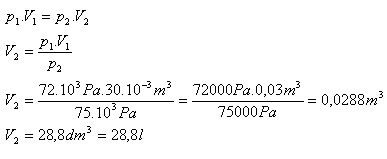
Nach der Druckerhöhung wird die Luft ein Volumen von 28,8 Liter haben.
3.Die Dichte von Helium beträgt bei einem Druck von 105 Pa ρ1 = 0,164 kg·m-3. Wie groß ist seine Dichte, wenn wir es auf einen Druck von 5·107 Pa komprimieren? (Masse und Temperatur des Gases ändern sich während der Kompression nicht).
Lösung:
Analyse:
p1 = 105 Pa, ρ1 = 0,164 kg·m-3 , p2 = 5·107 Pa, ρ2 = ?
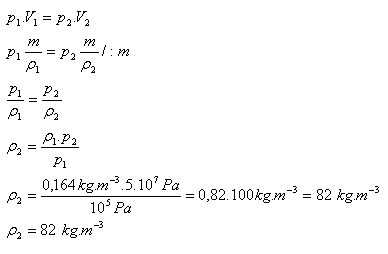
Die Dichte von Helium beträgt nach der Kompression 82 kg·m-3.
4.Die Dichte der Luft unter Normalbedingungen beträgt ρ1 = 1,3 kg·m-3. Wie groß ist die Dichte der Luft, wenn wir sie von Normalbedingungen auf 30oC erwärmen? (Die Menge der Luft ändert sich nicht).
Lösung:
Analyse:
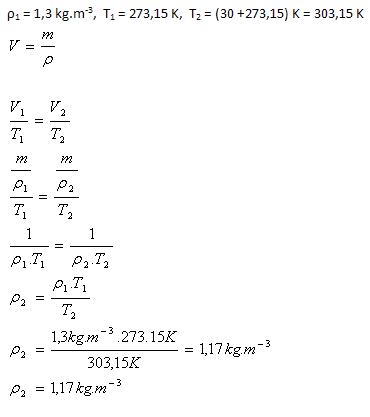
Die Dichte der Luft beträgt 1,17 kg·m-3.
5.Ein in einem Behälter mit beweglichem Kolben eingeschlossenes Gas wird bei konstantem Druck von 22oC auf 52oC erwärmt. Um wie viel Prozent hat sich sein Volumen vergrößert?
Lösung:
Analyse:
T1 = 295,15 K, T2 = 322,15 K, Δ% = ?
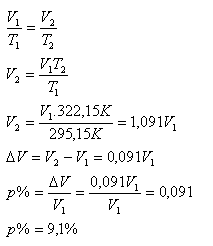
Das Volumen des Gases hat sich nach dem Erwärmen um 9,1 % vergrößert.
6. Eine Glühlampe wird bei der Herstellung mit Stickstoff bei einem Druck von 50,6 kPa und einer Temperatur von 18oC gefüllt. Welche Temperatur hat der Stickstoff in der leuchtenden Lampe, wenn sein Druck auf 118 kPa ansteigt?
Lösung:
Analyse:
p1 = 50,6 kPa = 50,6·103 Pa, T1 = 291,15 K, p2 = 118 kPa = 118·103 Pa, T2 =?
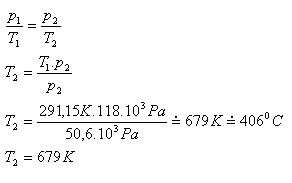
Die Temperatur des Stickstoffs in der leuchtenden Lampe beträgt ungefähr 679 K.
7.Bei einem Formel-1-Rennen stieg die Temperatur der Luft in den Reifen von 19oC auf 79oC. Wie ändert sich der Druck im Reifen, wenn er ursprünglich auf 240 kPa aufgepumpt war? Warum wird vor dem Start eine „Formationsrunde“ gefahren? (Das Innenvolumen des Reifens ändert sich nicht.)
Lösung:
Analyse:
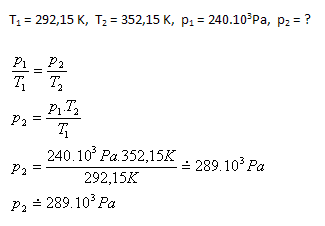
Der Luftdruck im Reifen steigt nach dem Erwärmen auf etwa 289 kPa. Die Formationsrunde sorgt dafür, dass es direkt beim Start nicht zu einem plötzlichen starken Anstieg des Reifendrucks und damit der Reifentemperatur kommt.
8.In einer zylindrischen Kammer befindet sich Luft, die von einem beweglichen Kolben in 50 cm Abstand vom Boden des Zylinders eingeschlossen ist. Der Luftdruck beträgt 105 Pa. Wird der Kolben bei adiabatischer Kompression um 20 cm in Richtung Boden bewegt, steigt der Luftdruck auf 2,05·105 Pa. Bestimmen Sie die Poisson-Konstante für Luft!
Lösung:
Analyse:
h1 = 0,5 m, V1 = 0,5S, h2 = 0,3 m, V2 = 0,3S, p1 = 105 Pa,
p2 = 2,05·105 Pa, κ = ?
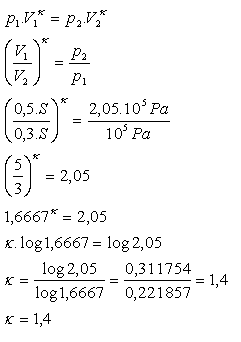
Die Poisson-Konstante für Luft ist κ = 1,4.
9.Zeigen Sie, dass für einen adiabatischen Prozess T1·V1κ-1 = T2·V2κ-1 gilt.
Lösung:
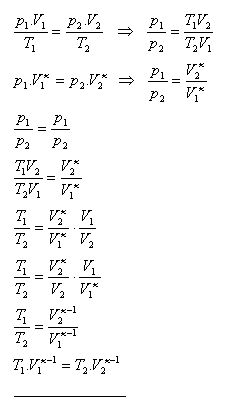
10. Bei adiabatischer Kompression wurde das Volumen der Luft auf 1/10 des ursprünglichen Volumens verringert. Berechnen Sie Druck und Temperatur der Luft nach der adiabatischen Kompression. Der Anfangsdruck der Luft betrug 105 Pa, die Anfangstemperatur 20oC. κ (Luft) = 1,4
Lösung:
Analyse:
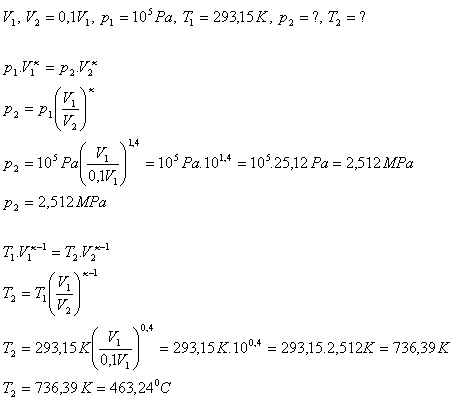
Nach der adiabatischen Kompression stieg der Luftdruck auf 2,512 MPa, die Temperatur auf 463,24oC.