Elektrický proud v elektrolytech
1.Charakterizujte elektrický proud v elektrolytech!
Řešení:
Elektrolyty jsou látky, jejichž roztoky nebo taveniny vedou elektrický proud pomocí iontů. Elektrický proud v elektrolytech je uspořádaným pohybem kationtů (+) a aniontů (-). Kationty se pohybují na katodu (-), anionty na anodu (+). Elektrolytická disociace je proces, při kterém se neutrálně molekuly elektrlytu štěpí na ionty. Elektrolýza je proces, při kterém nastávají chemické změny elektrod a elektrolytu, pokud jím prochází elektrický proud.

2.Vypočítejte:
- a.) množství hliníku, který se vyloučí při elektrolýze na elektrodě za 24 hodin proudem 10kA.
A(Al3+) = 0,093.10-6kg.C-1 - b.) jakým proudem by se vyloučil z elektrolytu chrom s hmotností 3,24 g za 1 hodinu
A(Cr3+) = 0,18.10-6kg.C-1
Řešení:

- a.) Na elektrodě se vyloučí 80kg hliníku.
- b.) Chrom se na elektrodě vyloučí proudem 5A.
3.Určete elektrochemický ekvivalent hliníku a mědi
Řešení:
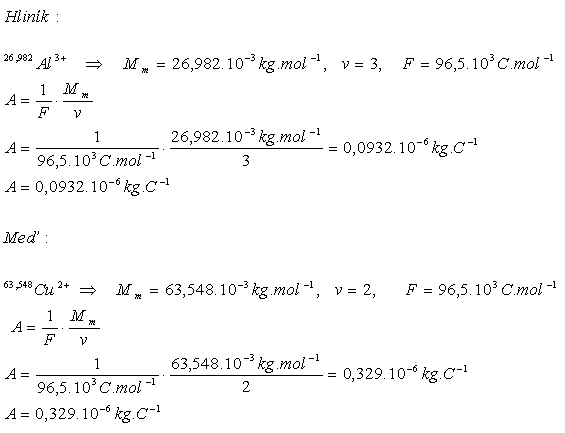
Elektrochemické ekvivalenty jsou A(Al)= 0,0932.10-6kg.C-1 a A(Cu)=0,329.10-6kg.C-1
4.Elektrolytem CuSO4 prochází proud 1A. Kolik atomů mědi se vyloučí na katodě za 10 sekund?
A(Cu) = 0,329.10-6kg.C-1 NA = 6,022.1023mol-1, Mm = 63,548.10-6kg.mol-1
Pro zobrazení řešení se přihlaste.5. Koule, jejíž poloměr je r = 5cm, má být poniklovaná vrstvou tloušťky h = 0,15 mm. Jak dlouho třeba kouli ponechat v elektrolytu při proudu I = 1A?
Pro zobrazení řešení se přihlaste.
6.Poniklování kovové destičky, která má povrch 100cm2, trvalo při proudu 0,4 A čtyři hodiny. Vypočtěte tloušťku niklové vrstvy, která se na destičce vytvořila!
Pro zobrazení řešení se přihlaste.7.Jakou energii potřebujeme, abychom při elektrolýze síranu měďnatého CuSO4 získali měď o hmotnosti 1g, pokud elektrolýza probíhá při napětí 4V?
Pro zobrazení řešení se přihlaste.
8.Dvě elektrolytické vany s roztoky AgNO3 a CuSO4 jsou zapojeny sériově. Kolik mědi se vyloučí za dobu, za kterou se vyloučí 850 mg stříbra?
Pro zobrazení řešení se přihlaste.9.Jaký elektrický proud procházel elektrolytem, když měděná katoda vážila před měřením 35g a po měření, které trvalo 40 minut 39g.
Pro zobrazení řešení se přihlaste.
10.Rozkladné napětí při elektrolýze kyseliny sírové mělo hodnotu 2,2 V. Při napětí 3,5 V procházel elektrolytem proud 2,8 A. Elektrody byly od sebe vzdáleny 4cm a průřez elektrolytického vodiče byl 30cm2. Určitě měrný odpor (odpor) elektrolytu!
Pro zobrazení řešení se přihlaste.
11.Za jaký čas se vyloučí z roztoku CuSO4 měď s hmotností 1,778 g proudem 3A?
Pro zobrazení řešení se přihlaste.12.Při elektrolýze modré skalice CuSO4 se na katodě za 2 hodiny vyloučí dvojmocných měď s hmotností
m = 9,504 g, Ampérmetr ukázal proud IA = 4,1 A. Zjistěte chybu ampérmetru ΔI.
13.Dvě elektrolytické nádoby s roztoky AgNO3 a CuSO4 jsou sériově spojeny. Určitě hmotnost mědi, která se při elektrolýze vyloučí za čas, za který se v druhé nádobě vyloučilo stříbro s hmotností 180g.
Pro zobrazení řešení se přihlaste.14.Při elektrolýze ZnSO4 se za 1 hodinu vyloučí zinek s hmotností m = 2,45 g. Určitě elektrický odpor roztoku, pokud napětí ně elektrodách bylo U = 6V.
Pro zobrazení řešení se přihlaste.15.Předmět s povrchem S = 20 dm2 je třeba postříbřit vrstvou o tloušťce h = 0,2 mm. Jak dlouho bude trvat pokovování, pokud 1 dm2 plochy může být zatížen proudem I = 0,4 A?
Pro zobrazení řešení se přihlaste.
16.Jakou energii potřebujeme, abychom při elektrolýze síranu měďnatého CuSO4 získali měď o hmotnosti
m = 1g, pokud elektrolýza proběhla při napětí U = 4V.
17.Roztokem CuSO4 prochází proud I = 1A. Kolik atomů mědi se vyloučí na katodě za t = 1s? (z = 2)
Pro zobrazení řešení se přihlaste.18. Jaký je elektrický náboj jednoho Iona stříbra, které se vyloučí elektrolýzou dusičnanu stříbrného nábojem Q = 1C.
Pro zobrazení řešení se přihlaste.19. Kolik a.) Stříbra b.) Dvojmocné mědi se vyloučí z příslušných roztoků pokud jimi projde náboj Q = 96,5.106C?
Pro zobrazení řešení se přihlaste.
20.Akumulátor se nabíjel proudem I1 = 5A po dobu t1 = 6 hodin. Jak dlouho se vybíjel, jestliže se při vybíjení odebíral z akumulátoru stálý proud I2 = 0,05 A. Nábojová účinnost akumulátoru je η = 90%.
Pro zobrazení řešení se přihlaste.