Elektrický prúd v elektrolytoch
1.Charakterizujte elektrický prúd v elektrolytoch!
Riešenie:
Elektrolyty sú látky, ktorých roztoky alebo taveniny vedú elektrický prúd pomocou iónov. Elektrický prúd v elektrolytoch je usporiadaným pohybom katiónov (+) a aniónov (-). Katióny sa pohybujú na katódu (-), anióny na anódu (+). Elektrolytická disociácia je proces, pri ktorom sa neutrálne molekuly elektrlytu štiepia na ióny. Elektrolýza je proces, pri ktorom nastávajú chemické zmeny elektród a elektrolytu, ak ním prechádza elektrický prúd.

2.Vypočítajte:
- a.) množstvo hliníka, ktorý sa vylúči pri elektrolýze na elektróde za 24 hodín prúdom 10kA.
A(Al3+) = 0,093.10-6kg.C-1 - b.) akým prúdom by sa vylúčil z elektrolytu chróm s hmotnosťou 3,24g za 1hodinu.
A(Cr3+) = 0,18.10-6kg.C-1
Riešenie:

- a.) Na elektróde sa vylúči 80kg hliníka.
- b.) Chróm sa na elektróde vylúči prúdom 5A.
3.Určite elektrochemický ekvivalent hliníka a medi
Riešenie:
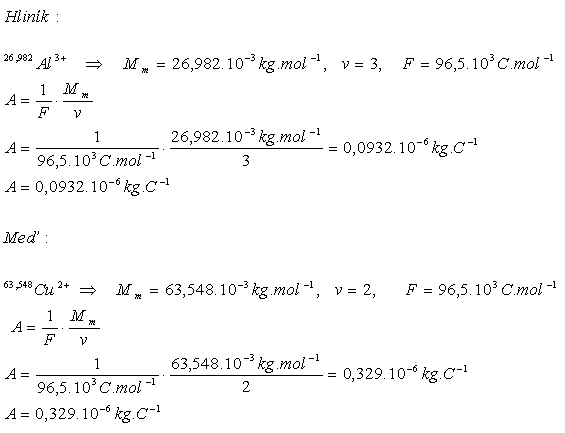
Elektrochemické ekvivalenty sú A(Al)= 0,0932.10-6kg.C-1 a A(Cu)=0,329.10-6kg.C-1
4.Elektrolytom CuSO4 prechádza prúd 1A. Koľko atómov medi sa vylúči na katóde za 10 sekúnd? A(Cu) = 0,329.10-6kg.C-1 NA = 6,022.1023mol-1, Mm = 63,548.10-6kg.mol-1
Prihláste sa pre zobrazenie riešenia5. Guľa, ktorej polomer je r = 5cm, má byť poniklovaná vrstvou hrúbky h = 0,15mm. Ako dlho treba guľu ponechať v elektrolyte pri prúde I = 1A?
Prihláste sa pre zobrazenie riešenia
6.Poniklovanie kovovej doštičky, ktorá má povrch 100cm2, trvalo pri prúde 0,4A štyri hodiny. Vypočítajte hrúbku niklovej vrstvy, ktorá sa na doštičke vytvorila!
Prihláste sa pre zobrazenie riešenia7.Akú energiu potrebujeme, aby sme pri elektrolýze síranu meďnatého CuSO4 získali meď o hmotnosti 1g, ak elektrolýza prebieha pri napätí 4V?
Prihláste sa pre zobrazenie riešenia
8.Dve elektrolytické vane s roztokmi AgNO3 a CuSO4 sú zapojené sériovo. Koľko medi sa vylúči za dobu, za ktorú sa vylúči 850 mg striebra?
Prihláste sa pre zobrazenie riešenia9.Aký elektrický prúd prechádzal elektrolytom, keď medená katóda vážila pred meraním 35g a po meraní, ktoré trvalo 40 minút 39g.
Prihláste sa pre zobrazenie riešenia
10.Rozkladné napätie pri elektrolýze kyseliny sírovej malo hodnotu 2,2V. Pri napätí 3,5V prechádzal elektrolytom prúd 2,8A. Elektródy boli od seba vzdialené 4cm a prierez elektrolytického vodiča bol 30cm2. Určite merný odpor (rezistivitu) elektrolytu!
Prihláste sa pre zobrazenie riešenia
11.Za aký čas sa vylúči z roztoku CuSO4 meď s hmotnosťou 1,778g prúdom 3A?
Prihláste sa pre zobrazenie riešenia12.Pri elektrolýze modrej skalice CuSO4 sa na katóde za 2 hodiny vylúči dvojmocná meď s hmotnosťou m = 9,504g, Ampérmeter ukázal prúd IA = 4,1A. Zistite chybu ampérmetra ΔI.
Prihláste sa pre zobrazenie riešenia13.Dve elektrolytické nádoby s roztokmi AgNO3 a CuSO4 sú sériovo spojené. Určite hmotnosť medi, ktorá sa pri elektrolýze vylúči za čas, za ktorý sa v druhej nádobe vylúčilo striebro s hmotnosťou 180g.
Prihláste sa pre zobrazenie riešenia14.Pri elektrolýze ZnSO4 sa za 1 hodinu vylúči zinok s hmotnosťou m = 2,45g. Určite elektrický odpor roztoku, ak napätie ne elektródach bolo U = 6V.
Prihláste sa pre zobrazenie riešenia15.Predmet s povrchom S = 20 dm2 je treba postriebriť vrstvou o hrúbke h = 0,2mm. Ako dlho bude trvať pokovovanie, ak 1 dm2 plochy môže byť zaťažený prúdom I = 0,4A?
Prihláste sa pre zobrazenie riešenia
16.Akú energiu potrebujeme, aby sme pri elektrolýze síranu meďnatého CuSO4 získali meď o hmotnosti m = 1g, ak elektrolýza prebehla pri napätí U = 4V.
Prihláste sa pre zobrazenie riešenia17.Roztokom CuSO4 prechádza prúd I = 1A. Koľko atómov medi sa vylúči na katóde za t = 1s? (z = 2)
Prihláste sa pre zobrazenie riešenia18. Aký je elektrický náboj jedného ióna striebra, ktoré sa vylúči elektrolýzou dusičnanu strieborného nábojom Q = 1C.
Prihláste sa pre zobrazenie riešenia19. Koľko a.) striebra b.) dvojmocnej medi sa vylúči z príslušných roztokov ak nimi prejde náboj Q = 96,5.106C?
Prihláste sa pre zobrazenie riešenia
20.Akumulátor sa nabíjal prúdom I1 = 5A po dobu t1 = 6 hodín. Ako dlho sa vybíjal, ak sa pri vybíjaní odoberal z akumulátora stály prúd I2 = 0,05A. Nábojová účinnosť akumulátora je η = 90%.
Prihláste sa pre zobrazenie riešenia